к.мед.н. нейрофізіолог невролог Олексюк-Нехамес А.Г.
Нервово-м’язова система являє собою функціонально тісно зв’язаний комплекс кістякових м’язів і сегментарних периферичних утворень нервової системи (сегментарні мотонейрони і рухові периферичні нервові волокна), що забезпечують їхню іннервацію. Функціональною одиницею нервово-м’язової системи є рухова одиниця (РО), що складається з одного мотонейрона, його аксона і м’язових волокон що їм іннервуються. М’язові волокна, що відносяться до території однієї РУ, функціонують як єдине ціле за принципом «усі чи нічого».Територія РО на поперечному зрізі наближається до кола і, як правило, «перекривається» територіями двох-трьох інших РУ.Одним з базових понять у электронейроміографії є рухова одиниця.Рухова одиниця (РУ) – це функціональна одиниця нейромоторного апарату, представляє собою групу м’язових волокон, що іннервується одним мотонейроном передніх рогів спинного чи мозку рухових ядер мозкового стовбура. У залежності від функціонального призначення РУ можуть включати різне число м’язових волокон: від 10—25 у дрібних м’язах до 2000 у великих м’язах, що несуть основне антигравітаційне навантаження.Гладке і більш-менш тривале скорочення м’яза в природних умовах забезпечується асинхронною роботою різних РУ з різними територіями.Нарощування сили скорочення здійснюється спочатку підключенням нових рухових одиниць (РУ), а потім і збільшенням частоти імпульсації по рухових аксонах, cкерованих на інтенсифікацію роботи.З функціональної точки зору РО розділяють на 2 основних типи: повільні (I тип) і швидкі (II тип).Повільні рухові одиниці (РО) включають повільний мотонейрон, що іннервує однотипні повільні м’язові волокна, швидкі РО — відповідно швидкі мотонейрони і швидкі м’язові волокна. У межах одного м’язу РО, що мають меншу територію, є повільними, і, навпаки, великі РО є швидкими.Повільні мотонейрони, як правило, малі по величині; вони характеризуються високою збудливістю, низьким порогом включення в імпульсну активність, відносно низкою частотою импульсації, вузьким частотним діапазоном між мінімальною і максимальною частотою импульсации, порівняно невисокою швидкістю проведення імпульсу по аксоні (і його меншим діаметром), високою витривалістю, нестомлюваністю.Швидкі мотонейрони — більш великі по величині клітини з більш товстим аксоном — характеризуються у порівнянні з повільними мотонейронами більш низькою збудливістю і високим порогом включення в імпульсну активність, вони використовуються лише при необхідності створення щодо великих по силі статичних і динамічних м’язових скорочень, а також швидкісних напруг з високим градієнтом сили. Нестомлюваність “повільних” мотонейронов обумовлене здатністю їх довгостроково (протягом десяток хвилин) підтримувати стабільно низькочастотну импульсацію без зниження її частоти. Швидкі мотонейрони відносяться до «швидко стомлюваних», оскільки не можуть стійко підтримувати високочастотну импульсацію: слідом за високочастотним розрядом настає більш-менш швидке падіння частоти. У залежності від швидкості зниження частоти импульсації швидкі мотонейроны поділяють на 2 підтипи: підтип ІІА — стомлюються повільно (частота імпульсації знижується повільно) і підтип ІІБ — стомлюються швидко (частота импульсації знижується швидко).Два підтипи швидких мотонейронов мають і інші розходження — у порозі порушення, частотному діапазоні импульсації.Відповідно швидким і повільної РУ м’язові волокна, що входять у їхній склад, відносяться до швидких чи повільних.Варто знати сучасні уявлення про структуру і біохімію основного складного елементу м’язової тканини — м’язове волокно і механізми його скорочення.Таким чином: загальне число м’язових волокон у людини відносно стабільно — воно наростає лише протягом першого півріччя життя.Внутрішній вміст волокна — цитоплазма — складається з ендоплазматичного матриксу і Ендоплазматичного ретикулуму. Ендоплазматичний матрикс можна уявити у вигляді внутрішньоклітинної рідини, у яку занурені скорочувальні елементи волокна — міофібрилли.Ендоплазматичний ретикулум — складна система подовжніх і поперечних трубочок і мішечків, покритих мембраною, аналогічної плазмолемі і, очевидно, що являється відгалуженням плазмолемми у глибину волокна.Паралельно росту дитини збільшується товщина волокон, що у дорослих приблизно в 5 разів більше, ніж у немовлят.М’язове волокно покрите мембраною — плазмолеммою.Міофибрилла — ниткоподібний утвір діаметром 1—3 мкм. Усього м’язове волокно містить до 1000 і більш міофибрилл.Міофибрилла складається з пучка паралельних товстих міозинових і тонких актинових міофіламентів (ниток), розташованих на поперечному зрізі міофібрилл гексагонально: актинова нитка оточена трьома міозиновими, а міозиновая — шістьма актиновими.Діючою одиницею міофібрилли є саркомер — проміжок між двома 2-лініями.Таким чином, міофибрилла — це ланцюжок саркомеров, ніби «прикладених» один до одної — кінець у кінець. Саме вкорочення саркомера визначає скорочення міофибрилл, м’язових волокон і всього м’яза.Поділ м’язових волокон на швидкі і повільні, тобто величина швидкості скорочення їх, насамперед залежить від активності міозин-АТФ-ази.Швидкі м’язові волокна з високою активністю цього ферменту відрізняються більш високою швидкістю скорочення — більш швидким замиканням і розмиканням поперечних містків з актином у порівнянні з повільними волокна. Не володіючи здатністю до швидких скорочень, повільні волокна відрізняються значно більшою витривалістю — здатністю до виконання тривалої роботи.Швидкі волокна на відміну від повільних характеризуються високою активністю гліколітичних ферментів (фосфофрукто-кінази), і великим змістом глікогену, що визначає їхню здатність до швидким і сильним, але нетривалим скороченням.Будь-який кістковий м’яз, як правило, містить і швидкі і повільні м’язові волокна, але співвідношення їх знаходиться у широких межах у залежності від характеру роботи, що виконує даний м’яз, віку, межі індивідуальних особливостей рухової характеристики людини. Швидкі волокна переважають у м’язах, яким потрібно велика швидкість скорочення і максимальна сила, що розвивається в короткий проміжок часу (високий «градієнт сили»).Навпаки, повільні волокна переважають у м’язах, призначених до виконання тривалої роботи зі стабільним, але невисоким зусиллям.Швидкі волокна васкуляризуются меншим числом капілярів, зміст у них мітохондрій, міоглобіну і жирів нижче, ніж у повільних м’язових волокнах. Так само як і «швидкі» мотонейрони, швидкі м’язові волокна поділяються на два підтипи.Процентний вміст швидких волокон залишається найбільш високим у активному віці — від 20 до 40 років (близько 60 %), після 40 років загальне число швидких волокон поступово зменшується, а після 60 років переважають повільні волокна (55%), що відповідає динаміці вікової трансформації рухової активності.
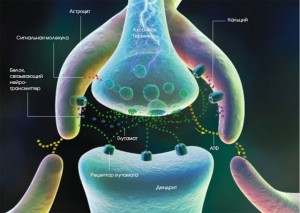
Товщина швидких волокон також починає зменшуватися після 40 років і до 60 років падає приблизно в 1,5 рази, у той час як товщина повільних волокон залишається щодо стабільної протягом життя, зниження намічається лише після 60 років.Пучок м’язових волокон одної ПРО – при міодистрофіях.Нервово-м’язова передача, тобто передача імпульсу від аксона мотонейрона на м’язове волокно, здійснюється не безупинно, а за допомогою нервово-м’язового синапса, що є не пасивною «переправою» сигналу, а активно бере участь у регуляції кількості і частоти сигналів, що переправляються.Отже, нервово-м’язовий синапс — це тонка щілина, укладена між пресинаптической мембраною (мембраною кінцевої гілочки рухового аксона) і постсинаптичною мембраною (мембраною м’язового волокна) чи кінцевою пластинкою. В області кінцевої пластинки плазмолемма утворює численні складки, що збільшують її поверхню.
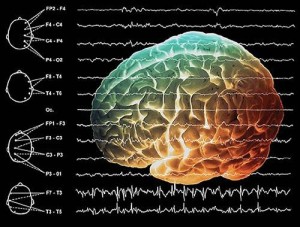
Поширення нервового імпульсу по аксоні.Проведення імпульсу по мієлінізованному нервовому волокну.Пресинаптична мембрана виділяє медіатор ацетилхолін, міхурці якого містяться у величезній кількості в кінцевих закінченнях аксона, а постсинаптична мембрана має у своєму розпорядженні особливі, чутливі до ацетилхоліну рецептори, але одночасно містить фермент ацетилхолинестеразу, здатну руйнувати ацетилхолін. МЕХАНІЗМ ВИНИКНЕННЯ І ПРОВЕДЕННЯ НЕРВОВОГО ІМПУЛЬСУ.При подразненні нервової клітки виникає швидке коливання величини мембранного потенціалу, що відповідає утворенню потенціалу дії (ПД).При цьому, проникність мембрани для іонів натрію різко підвищується і стає в десятки разів вище проникності для іонів калію: швидкісний потік іонів натрію всередину клітини значно переважає над зворотним потоком іонів калію.У зв’язку з цим виникає реверсія мембранного потенціалу, що відповідає висхідній частині кривої потенціалу дії (ПД) — фазі деполяризації.Висока проникність мембрани для іонів натрію триває усього частки мілісекунди, слідом за чим проникність для іонів натрію знижується, а для іонів калію підвищується.Включення в роботу натрій-калієвого насосу приводить до видалення іонів натрію з протоплазми і «накопичуванню» всередину клітини іонів калію: відновлюється звичайне іонне співвідношення по ободва боки мембрани і вихідний рівень поляризації (потенціал спокою).
(ПД, потенціал дії) виникає тільки за умови деполяризації до визначеного критичного рівня деполяризації — неоднакового в різних ділянках нейрона.Чим вище поріг деполяризації, тим нижче збудливість мембрани і навпаки.При подразненні аксона достатня деполяризація на 5-10 мв, при подразненні тіла нейрона необхідна деполяризація на 20—35 мв.При дії подразника діє закон «все чи нічого»: якщо подразнення підпорогове, ПД не виникає, якщо надмежове — розвивається максимальна для даних умов амплітуда ПД.При виникненні ПД у визначеній ділянці мембрани тіла чи нейрона його аксона створюється різниця потенціалів між збудженою ділянкою і незбудженим сусідньої — з’являються місцеві струми, що приводять до деполяризації сусідньої (незбудженої) ділянки мембрани, підвищенню її проникності для іонів натрію і створенню тут нового потенціалу дії -ПД. Принцип генерації потенціалу дії рухової одиниці ПД РО (А, Б, В, — мотонейрони переднього рогу спинного мозку; 1-5 м’язові волокна, що відносяться до території інервації мотонейрону. Оскільки в ділянці вихідного порушення в цей період настає рефрактерная фаза і відновлюється потенціал спокою, то створюється враження зсуву ПД з однієї ділянки на сусідній.
Насправді поширення імпульсу по аксоні — це не зсув одного ПД, а багаторазове виникнення нових ПД на сусідніх відрізках мембрани аксона по його ходу.Імпульс може поширюватися (проводитися) по аксоні в обидва боки – ортодромно* (від тіла нейрона) і антидромно (назад до тіла нейрона), однак властивість рефрактерности нейрона визначає в нормі «загасання» антидромного сигналу.Таким чином, проведення імпульсу по аксоні відбувається за рахунок місцевих струмів, і, отже, швидкість проведення імпульсу (СПИ) насамперед визначається властивостями нервового волокна (аксоплазмы і мембрани) і навколишньої волокно середовища. (згодом буде вивчатися ортодромна і антидромна методика накладання електродів)